3,3’-二芳基联萘酚骨架是联萘酚衍生的手性配体和催化剂中的结构基础,这些配体和催化剂,比如手性磷酸,亚磷酰胺配体等已被广泛应用不对称反应中。而在这些反应中,3,3’位的芳基取代基对于手性环境的构建起到至关重要的作用,因此,如何方便快捷的在联萘酚的3,3’位引入芳基取代基成为研究热点。在已发展的方法学中,引入取代基时都需要对酚羟基进行保护和脱保护,反应路径长,效率低,因此发展联萘酚3,3’位碳氢键的直接芳基化反应仍然十分必要。
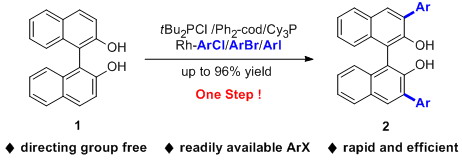
近期,南开大学元素有机国家重点实验室叶萌春教授小组成功实现了联萘酚类化合物3,3’位直接芳基化反应,一步高效的引入双芳基,成功避免了保护基/导向基的使用,大大提高了反应效率,能够以最高达96%的收率得到目标产物。
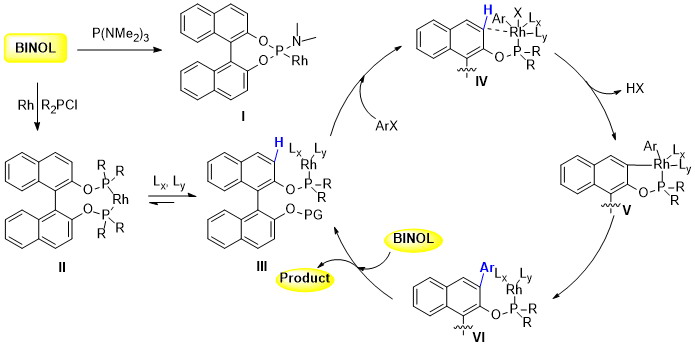
该小组也对于反应可能的路径进行了阐述,联萘酚与三(二甲基氨基)膦反应后与铑配位得到的配合物I由于金属铑与邻位碳氢键空间距离远,因此是没有反应活性的;而配合物II由于配位稳定,难以解离,因此也无法发生邻位碳氢键芳基化反应。但是,当额外加入配体三环己基膦时,它与铑发生竞争性配位从而使铑与原配体发生解离。金属铑靠近邻位碳氢键,得到活性的反应中间体III,随后发生氧化加成、碳氢键活化插入、还原消除得到3,3’位芳基化的产物,铑在与配体解离后进入下一循环。(Angew. Chem. Int. Ed. 2016, 55, doi:10.1002/anie.201607893)