手性邻二胺是一种广泛存在于具有生物活性的天然产物和药物中的重要结构单元。同时,过渡金属催化的不对称反应和有机催化所使用的手性配体和催化剂也含有该结构单元。因此,在过去的几十年中,开发有效的手性邻二胺的合成路线引起了研究者极大的兴趣。迄今为止,已经报道了许多基于不对称催化的合成方法。然而,大多数方法仍受限于底物范围较窄,需要吸电子基团进行保护,通过后续转化形成游离胺以及不能区分产物中两个氨基。因此,发展直接且原子经济的方法,通过简单的起始原料催化不对称合成具有结构多样性的未保护手性邻二胺具有很重要的意义。

不对称氢化是制备各种手性胺的最有效方法之一。然而,通过催化不对称氢化直接合成手性邻二胺的例子非常少见。2016年,范青华课题组报道了通过手性钌(二胺)催化的2,2’-双喹啉衍生物的不对称氢化,高对映选择性地合成了内环邻二胺。但是,该方法存在以下问题:一方面是底物合成较为困难,另一方面是大位阻底物的立体选择性较差。基于此,该课题组设想,通过分子间还原胺化和喹啉的不对称氢化串联反应,利用原料易得的2-喹啉醛和芳香胺来制备手性N,N’-二芳基邻二胺。该过程可能遇到三个挑战:1)二胺产物的强配位作用可能会使催化剂失活;2) 2-喹啉醛可能会被直接氢化;3)当使用空间位阻大的起始原料时,很难控制其对映选择性。
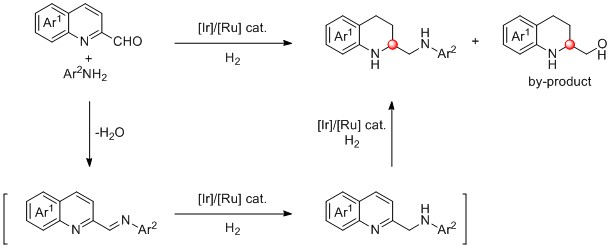
通过筛选溶剂,催化剂,反应温度和氢气压力。确定了最优的反应条件为:IPA (1.0 mL),cat. (5 mol%),25 oC,H2 (50 atm)。且发现铱和钌催化剂对不同的底物都能够获得较好的收率和优异的对映选择性。最终,作者通过铱或钌催化的2-喹啉醛和芳香胺的分子间还原胺化和不对称氢化的串联反应,以高收率(最高>95%)和优异的对映选择性(最高> 99% ee)获得了一系列位阻可调的手性N,N’-二芳基邻二胺。(Angew. Chem. Int. Ed. 2019, 58, 16831)(推荐人:白雨晴) (检查:翟小勇)
