三取代烯烃骨架广泛存在于天然产物和生物活性分子中,在合成中通常以三取代烯烃作为合成中间体来构建环丙烷、环氧化合物、氮丙啶和叔碳手性中心。三取代烯烃通常是通过羰基烯化,炔烃的氢官能化,交叉偶联,烯烃复分解来制备的(图1a)。尽管已经发展了上述方法,但当三取代烯烃各取代基的位阻和电子效应差别不大时,反应的区域和立体选择性的控制具有一定挑战。另外,非活化的1,2-二取代烯烃的直接官能化来制备不对称三取代烯烃得到了科学家们的广泛关注。当底物含有导向基团时,可以增强烯烃相邻位点C-H键的活性和位点选择性(图1b)。至今为止,钌、铑、钯、铱、铁和钴等过渡金属在由导向基控制的邻位C-H键活化官能团化反应中取得不错的进展,但是烯烃的远程C-H键活化官能团化仍是一个挑战性课题。
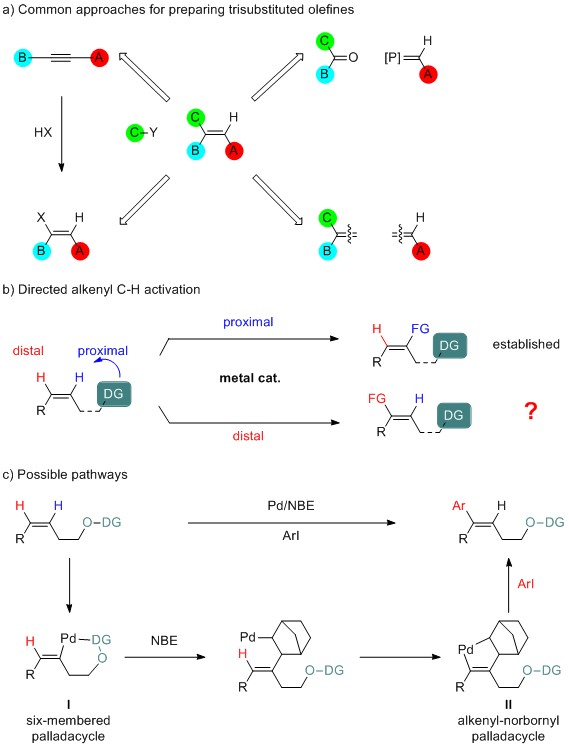
最近,钯/降冰片烯的催化体系有效应用于芳基的官能化。2015年,余金权和董广彬课题组分别报道了钯/降冰片烯催化的芳烃间位C-H键活化。因此作者设想这一策略能否被运用于烯烃底物。首先通过官能团导向的烯烃邻位C-H键活化,随后降冰片烯插入,并发生第二次烯烃远程C-H键活化生成物种II,物种II可以和亲电试剂反应,实现烯烃的远程C-H键活化官能化(图1c)。和芳烃相比,一些挑战存在于上述设想中。首先烯烃的π键更活泼,它可以和氧化剂或亲电试剂发生一系列副反应。其次,烯烃的π键比芳基更容易和金属钯配位,发生钯介导的2π-插入和亲核进攻反应,这会和第一次烯烃邻位C-H键活化发生竞争。最后,在降冰片烯插入后,烷基钯中间体通过迁移插入容易和烯烃形成环丙烷,这和烯烃的远程C-H键活化发生竞争,因此这类反应目前没有被实现。
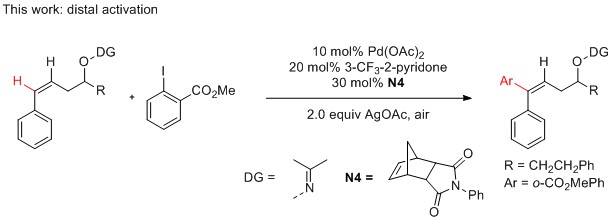
在此,美国芝加哥大学董广彬课题组发现使用合适的导向基,可以解决上述问题,通过钯/降冰片烯共催化实现烯烃的远程碳氢键活化官能化,来制备三取代烯烃(图2)。该反应具有很好的区域选择性和立体选择性,条件温和,可在空气中反应,底物适用性广,最高可实现84%的收率和专一的E式选择性,并且该反应可以进行克级规模试验。(DOI: 10.1021/jacs.9b11479) (推荐人:王晓清) (检查:赵洋)