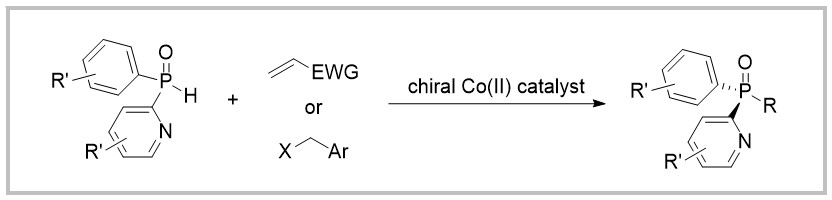
手性膦化合物作为配体或有机催化剂,在不对称合成中具有着重要的意义和价值。与轴手性、面手性和碳中心手性的含磷化合物相比,人们对于磷手性化合物的研究相对较少。较为主流的合成磷手性化合物的策略是使用手性辅助试剂,或对消旋体进行拆分。这些方法都需要使用当量的手性试剂。近期,相继有一些以不对称催化手段合成磷手性化合物的报道,例如通过C-H键活化、不对称加成及[2+2+2]环加成等。然而,在这些方法中,磷的强配位性可能会导致金属催化剂失活,进而导致反应的对映选择性降低。最近,陕西师范大学的段课题组报道了一种钴催化膦氧化合物的不对称亲核加成/烷基化反应,能够以最高99%的收率和99.5%的ee值获得手性膦氧化合物。
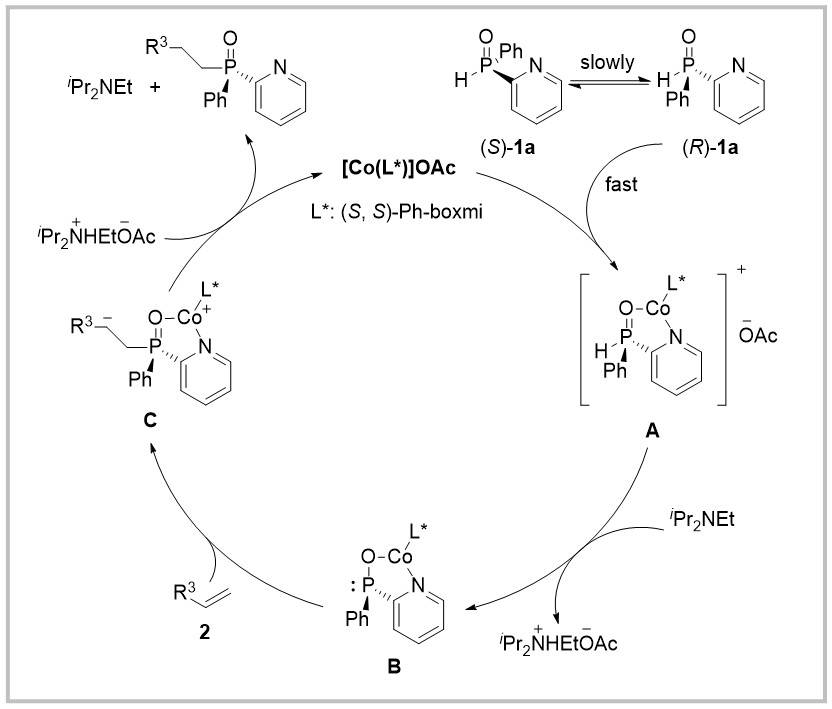
通过机理实验,作者推测具体的机理如下。首先,(R)-1a更容易与钴催化剂配位,产生中间体A,随后,体系中的碱使中间体A转化为中间体B,此时,与磷原子相连的苯环更偏向于处于远离配体的一侧,中间体C通过质子解即可得到最终产物,并再生钴催化剂。
Reference:Wu, Z.-H.; Cheng, A.-Q.; Yuan, M.; Zhao, Y.-X.; Yang, H.-L.; Wei, L.-H.; Wang, H.-Y.; Wang, T.; Zhang, Z.; Duan, W.-L. Cobalt-Catalysed Asymmetric Addition and Alkylation of Secondary Phosphine Oxides for the Synthesis of P-Stereogenic Compounds. Angew. Chem. Int. Ed. 2021, 60, 27241-27246. (推荐人:牛童 检查人:汤淏)