手性胺是有机合成及制药和农用化学品中的重要结构骨架。近来,通过不对称氢化的方法合成手性胺收到了广泛关注,其底物主要集中在亚胺和烯胺。当然,还原胺化作为一种直接、高效合成手性胺的方法,也备受关注。然而,目前为止,通过还原胺化的方法合成伯胺往往需要多步实现(如下图)。最近,Schaub及其合作者以氨气作为氮源,一步实现了烷基芳基酮的还原胺化,以最高87%的ee值实现了伯胺的化学选择性合成。
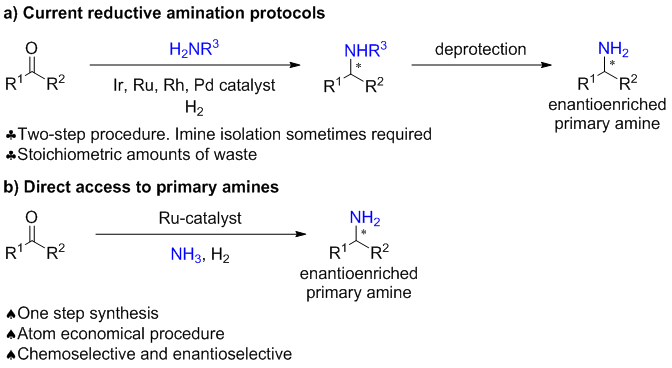
通过对配体、添加剂的筛选,最终确定反应的最优条件:以[Ru(Cl)H(CO)(PPh3)3)]为金属前体,(S,S)-f-binaphane为配体,NH4I为添加剂,同时加入2 mol%的NaPF6,120 oC甲苯条件下反应16小时。反应仅适用于烷基芳基酮,对于烷基烷基酮或者芳基芳基酮反映效果不好。

通过单晶、核磁以及理论计算,推测可能的机理如下:首先底物与钌进行配位,随后形成η2-配合物,之后Ru-H对底物进行对映选择性加成形成Ru-N键,氢气对Ru进行氧化加成,通过形成过渡态,之后形成Ru-H σ-配合物,最后还原消除(决速步)完成催化循环。(J. Am. Chem. Soc., Article ASAP DOI: 10.1021/jacs.7b10496)
