烷基亲电试剂与潜官能化亲核试剂(例如有机锌,有机硼,格氏试剂和有机硅烷试剂)之间的过渡金属催化交叉偶联反应已成为合成对映体富集产物最有力的方法之一。在这些反应中,α-卤代羰基化合物及其衍生物(例如腈,磺酸盐,磷酸盐,酰胺等)的偶联是值得注意的,因为所得的α-官能化的羰基化合物是有机合成中的通用结构单元。虽然对于羰基化合物α-官能化的C(sp3)和C(sp2)偶联反应已经取得了重大进展,但是对于C(sp)的偶联反应报道相对有限,这大概是因为炔烃容易发生副反应。鉴于内部炔烃是天然和生物活性分子以及功能材料中的重要单元,引入碳碳三键这一部分的方法学发展引起了合成界的持续关注。
2003年,Fu等人报道通过使用催化量的钯盐和铜盐并结合N-杂环卡宾配体,开创了一种将末端炔烃与未活化的伯溴化物和碘化物偶联的方法。这激发了化学家们探索其他金属-配体体系,以偶联更具挑战性的仲烷基卤化物和α-羰基卤化物。Lei研究小组等人报道了通过Pd催化的Stille和Suzuki反应,实现了炔金属物种(炔基锡烷和炔基三氟硼酸酯)与α-卤代羰基化合物的偶联。Li研究小组最近报道了末端炔烃和α-羰基卤化物的光催化偶联反应。尽管取得了这些进步,但据文献查阅,末端炔烃与α-羰基卤化物的不对称Sonogashira型偶联仅取得了有限的成功。Liu最近报道了在铜催化下,使用手性金鸡纳生物碱衍生的P,N-配体,实现了多种末端炔烃和外消旋烷基卤化物之间C(sp3)-C(sp)的Sonogashira交叉偶联反应,并且以α-溴酰胺为底物,能够获得良好的收率和ee值。鉴于α-炔基羰基化合物的重要性,仍然需要寻找一种可从市售化合物(如炔烃和α-卤代羰基化合物)直接得到高对映选择性的α-炔基羰基化合物的手性催化体系。在此,上海有机所张国柱研究员课题组报道了铜催化的不对称Sonogashira交叉偶联反应,使用α-卤代酰胺与未官能化的末端炔烃作为底物,合成了多种β,γ-炔基酰胺。

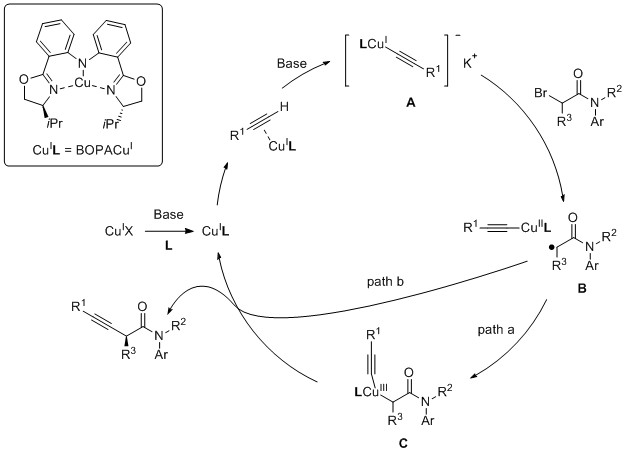
下图为作者提出的可能机理:在碱性条件下,Cu(I)X与L进行配体交换,生成三齿络合物Cu(I)L,随后,在K3PO4存在下与炔烃配位生成中间体A,中间体A可以还原α-溴酰胺,生成二价铜物种和烷基自由基B。最后,经历两种可能的途径:在途径a中,烷基自由基与二价铜反应生成三价铜络合物C,然后经还原消除得到目标化合物并再生催化剂;在途径b中,烷基自由基可能与二价铜物种直接通过笼外成键,从而提供相同的结果。(Angew. Chem. Int. Ed.2020, 59, 13998-14002.) (推荐人:白雨晴) (检查人:刘丽霞)