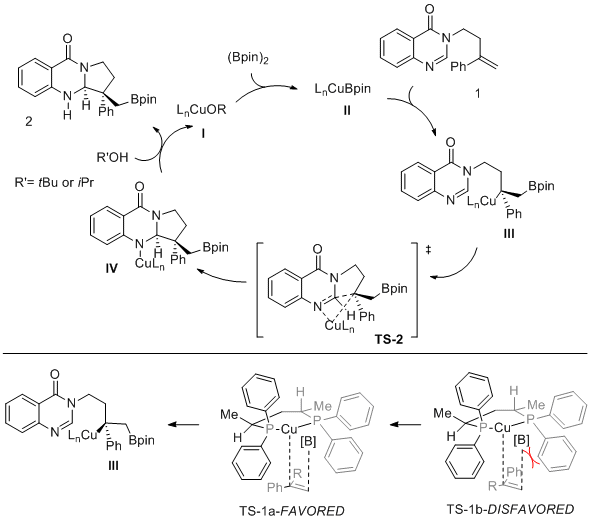
喹唑啉酮对映体具有不同的生物活性,因此对映选择性地制备此类化合物具有重要意义。目前手性喹唑啉酮类化合物的构建方法通常采用经典的手性拆分和手性池合成。在喹唑啉酮类化合物中,吡咯喹唑啉酮结构具有药物分子和天然产物中常见的三环骨架,但目前几乎没有构建手性吡咯喹唑啉酮的策略。因此探索对映选择性地构建吡咯喹唑啉酮骨架的方法是一个挑战。
铜催化的烯烃硼化官能化是构筑立体可控的复杂分子的有力手段,并且此方法可应用于环化反应。2018年以来,Yun等课题组已经使用这种策略成功构建了重要的含氮杂环化合物-吲哚啉。2020年,Lautens报道了铜催化的共轭borylation/Mannich环化反应,立体选择性地合成了四氢喹啉(Fig. 1A)。此研究表明了铜催化硼化环化反应的如下潜力:(1)形成几个高度可控的立体中心;(2)引入可衍生化的含硼官能团;(3)制备一系列含氮杂环化合物。基于以上研究,最近Procter报道了铜催化硼化环化反应合成吡咯喹唑啉酮的方法(Fig. 1B),高对映和非对映选择性地构建了两个相邻的立体中心,并通过随后的衍生化,制备多种具有潜在生物活性的喹唑啉酮衍生物。
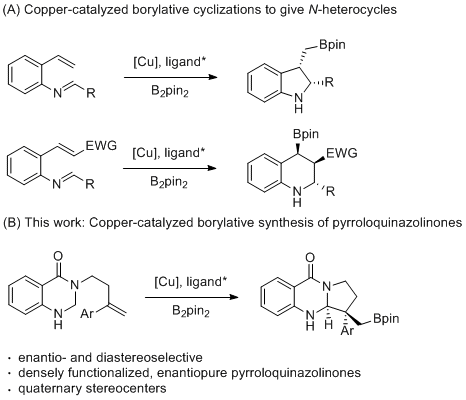
作者推测反应机理如下:首先催化活性物种I与联硼酸频哪醇酯反应生成铜-硼物种II,随后对映选择性地插入至底物的碳碳双键上得到III。立体化学模型表明,底物中苯基与手性配体位阻起主导作用(TS-1a vs. TS-1b),可以高对映选择性地得到烷基铜中间体III。烷基铜中间体III继续迁移插入至底物的碳氮双键,生成中间体IV。最后,中间体IV质子解得到目标产物,同时重生催化活性物种I,完成催化循环(Fig. 2)。( Angew. Chem. Int. Ed. 2021, 60, 14355 -14359.) (推荐人:荀珊珊) (检查:丁艺璇)