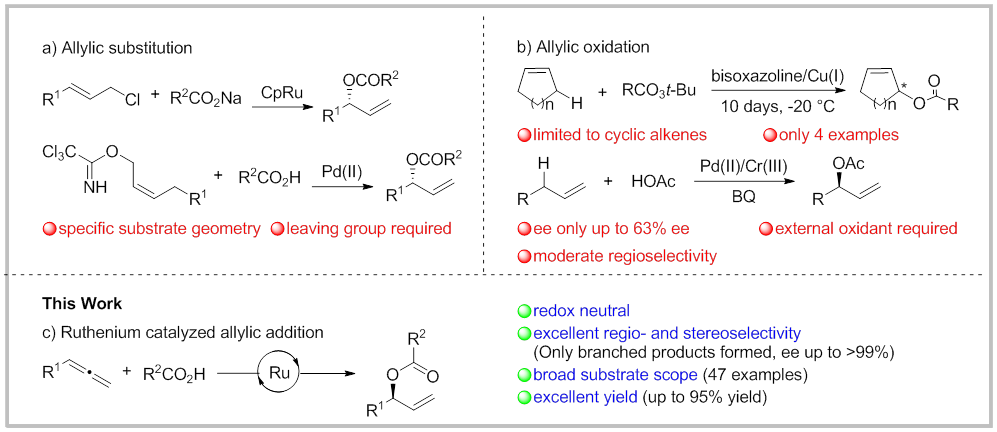
手性烯丙基酯是非常重要的有机合成子,广泛存在于天然产物中。传统上,该类化合物可以通过相应的烯丙醇的酰基化反应来制备。近年来,过渡金属催化的手性烯丙基酯的合成也取得了很大的进展。比如,通过烯丙基取代反应获得烯丙基酯,但这种方法对底物的Z/E构型要求很高,并且原子经济性低。此外,也可通过烯丙基C−H氧化的方法获得,但该方法需要化学计量的氧化剂,且底物适用范围窄,对映选择性也不佳。
为了克服上述合成方法的缺点,最近,Breit Bernhard课题组报道了在钌催化下,通过羧酸对联烯的不对称加成来制备手性烯丙基酯的方法。该方法使用了基于Josiphos骨架来设计并制备的配体,得到了具有良好区域选择性和高对映选择性的支链烯丙基酯,并且该反应具有广泛的底物范围和良好的官能团容忍性。
最后,作者给出了该反应的机理:首先,羧酸对Ru(II)络合物氧化加成生成Ru(IV)络合物(步骤I)。其中,Ru(IV)络合物和联烯中取代基较少的一侧发生快速可逆的氢金属化,以及紧随其后的β-氢消反应,生成Ru(IV)络合物。该过程通过氘代实验,可以在烯烃的末端观察到氘得以证实。接着,联烯中取代基更多的一侧与Ru(IV)络合物发生氢金属化反应形成Ru-π-烯丙基络合物(步骤II),最后,经过还原消除(步骤III)生成目标产物并释放Ru(II)络合物,完成催化循环。
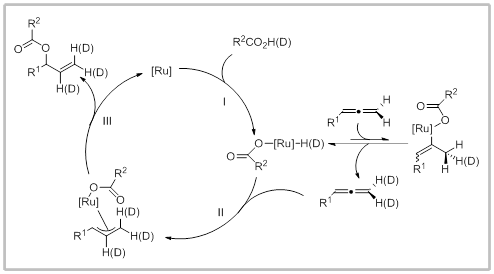
Reference: Hu, J.-L.; Bauer, F.; Breit B.* Ruthenium-Catalyzed Enantioselective Addition of Carboxylic Acids to Allenes. ACS Catal. 2021, 11, 19, 12301-12306.(推荐人:陈简,检查人:黄文君)