烯烃的催化氢胺化反应是构建广泛存在于各种生物活性天然产物和药物中的含氮化合物最方便、最快速的方法之一,因此在过去几十年中引起了合成界的广泛关注。在众多的方法中,过渡金属催化的烯烃自由基氢胺化具有高化学选择性、高反应活性、优异的官能团耐受性以及易于构建拥挤的碳中心等优点。虽然该领域取得了令人瞩目的进展,但在温和的条件下,开发一种通用且高效的对映选择性地烯烃自由基氢胺化反应,以获得有价值的手性胺,是一项持久且艰巨的挑战。
从机理上讲,过渡金属催化的自由基氢胺化反应可分为两类。其中一种方法涉及N-中心自由基触发的碳碳双键加成,然后是氢原子转移(HAT)过程。在此背景下,Knowles、Leonori和Xiao课题组在温和条件下利用各种N-中心自由基前体开发了一系列自由基氢胺化反应。另一种途径为金属氢化物介导的转化,其中原位生成的烷基自由基源于金属氢化物催化剂和碳碳双键之间的HAT,通常可分为两种情况:1)直接与氮基自由基试剂反应,例如硝基化合物、偶氮化合物,叠氮化合物和重氮化合物;2)利用各种含氮亲核试剂作为偶联剂进行自由基-极性交叉胺化反应。而迄今为止,只有少数氮基亲自由基试剂与这种金属氢化物介导的自由基氢胺化反应相容。相对地,有报道通过使用CoIIIH催化剂和合适的氧化剂原位生成烷基自由基,随后进一步转化为相应的亲电中间体,最后被含氮亲核试剂捕获生成相应的含氮化合物。
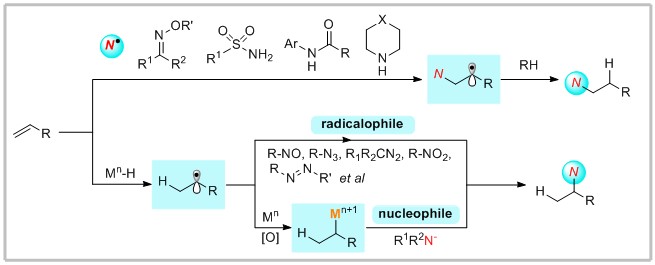
本文作者通过N-氟代双苯磺酰胺(NFSI)及其类似物实现了各种烯烃通用和高效的共催化自由基氢胺化方法,包括苯乙烯、烷基取代烯烃、张力烯烃以及α,β-不饱和羰基(例如醛、酮、酸、酯和酰胺)。总的来说,该反应具有独特的Markovnikov选择性和良好至优异的产率。此外,通过使用手性钴(II)-希夫碱催化剂,可以取得较好的对映选择性。
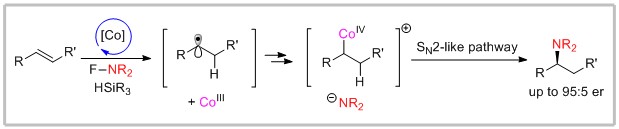
Reference: Qin, T.; Lv, G.; Meng, Q.; Zhang, G.;* Xiong, T.;* Zhang, Q.* Cobalt-Catalyzed Radical Hydroamination of Alkenes with N-Fluorobenzenesulfonimides. Angew. Chem. Int. Ed. 2021, 60, DOI: 10.1002/anie.202110178.(推荐人:丁艺璇,检查人:朱周豪)