Suzuki-Miyaura交叉偶联反应已成为有机和药物化学中不可或缺的工具,通过C-C键实现分子碎片间简单和稳固的结合。各种有机硼亲核试剂的当前可获性和相对稳定性赋予这些反应极大的操作简便性。Suzuki-Miyaura偶联剂最常用的亲电子试剂是有机卤化物和磺酸盐。Suzuki-Miyaura反应的发现和发展替代的亲电试剂具有重要意义,特别在传统的亲电试剂是惰性,不稳定或难以制备的情况下。在这方面,一些最近的成果包括使用酚盐,醚或酯,铵或吡啶盐,硝基化合物,酰胺,酰氟和活化的C-C键作为亲电试剂。这些进步极大地丰富了合成化学家的工具箱,可以合成更多的化合物。
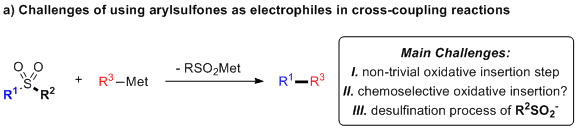
砜代表了化学中基本的官能团。砜的多功能性和稳定性使它们成为许多复杂产品的合成方案中应用的重要中间体。然而,与有机卤化物或磺酸盐相比,在交叉偶联反应中使用砜作为亲电试剂是相对少有的。有几个因素可能促成了这一结果。首先,较少极化的C-SO2R键的氧化插入比较困难。其次,砜含有两个C-SO2键,其必须在氧化插入步骤中有所区分。第三,在氧化插入时,所得的磺酸盐(RSO2-)容易脱硫得到R-,其可以作为亲核试剂而不是亲电试剂重新进入催化循环。
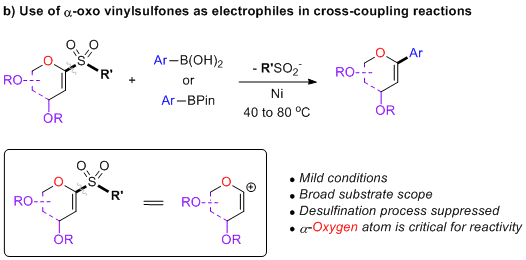
作者对开发合成糖类衍生物的新方法感兴趣。在一个旨在制备碳-芳基烯糖类(药学上重要的碳-糖苷的常用中间体)的项目中,对使用1-磺酰基烯糖作为相应的1-碘-烯糖亲电交叉偶联物的替代物的可能性感到好奇。作者在这项工作中确立了1-磺酰基烯糖可以在Ni催化的Suzuki-Miyaura反应中作为方便的亲电试剂,以高产率得到各种碳-芳基烯糖。作者进一步确定,无环α-氧代乙烯基砜也可以在这些反应中起到亲电合成子的作用,提供无环乙烯基醚。控制实验表明,α-氧原子在活化底物和促进所需反应方面起着关键作用。
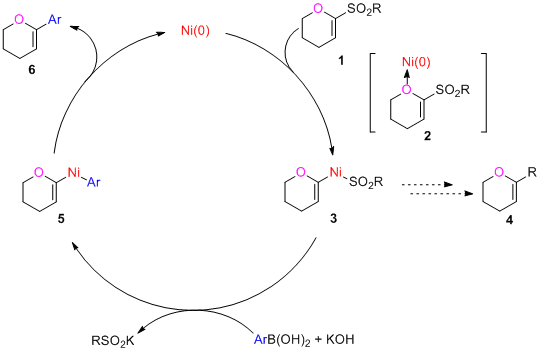
作者提出了如下合理的反应机制:底物1首先通过Ni(0)进行区域选择性C-S键插入,得到3,可能是由瞬时形成的2所促进的。乙烯基镍物种3可以经历脱硫以及还原消除以得到4,或者是转金属化得到5,然后还原消除,得到产物6。而作者的反应表明:转金属化过程的速率超过脱硫过程的速率。(HZ, J. Am. Chem. Soc., 2019, 141, 7680 )