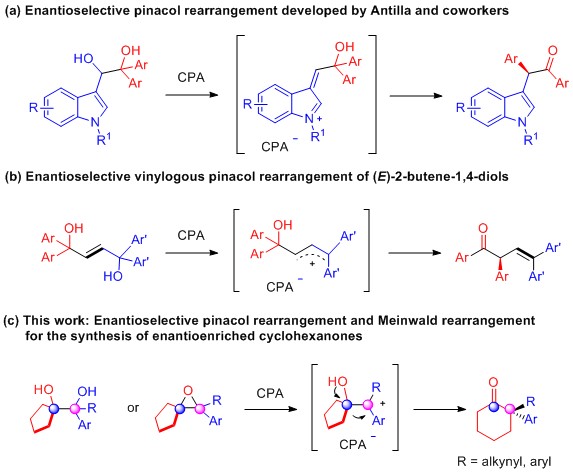
具有季碳中心的环己烷结构单元广泛存在于许多天然产物中,2位双取代的环己酮化合物是合成此类化合物的起始原料,因此得到化学工作者的广泛研究。Pinacol重排是指在酸性条件下1,2-二醇化合物重排得到醛或者酮化合物,在重排过程中可以产生一个新的手性中心。科研工作者在研究中发现经典的路易斯酸和布朗斯特酸由于无法与中间体和催化剂接触,所以难以实现手性控制。到目前为止,对于对映选择性的Pinacol重排反应只有两例报道。2010年,Antilla小组报道了手性膦酸催化地具有吲哚骨架二醇化合物的重排反应。随后,祝介平小组报道了(E)-丁烯-1,4-二醇的对映选择性乙烯基重排反应,可以得到β,γ-不饱和酮化合物。以上反应均经历了芳基的迁移重排,得到具有手性中心的链状酮化合物。后来,Snyder小组使用化学当量的手性膦酸催化合成了具有季碳手性中心的醛化合物。对于催化对映选择性重排反应合成具有手性季碳中心2位取代的双芳基和炔基/芳基环己酮化合物还未见报道。最近,祝介平课题组报道了对映选择性的Pinacol重排和Meinwald重排反应得到季碳中心的环己酮化合物。
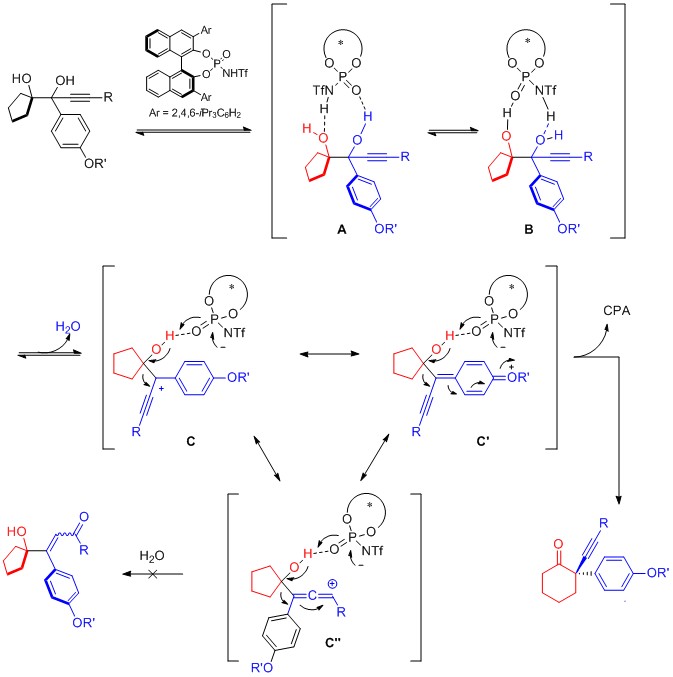
针对该反应,作者提出了可能的反应路径。手性膦酰胺作为双官能化催化剂可以与二醇形成分子间氢键,得到一个九元环中间体(A和B)。随后,中间体B可以脱除一分子的水,得到中间体C。炔基和富电子的芳基可以很好的稳定得到的碳正离子。中间体C经重排反应之后得到目标产物。在重排过程中并未得到副产物,说明分子内的芳基重排比分子内亲核捕获更快。(J. Am. Chem. Soc. 2019, 141, 11372)
(赵子彪推荐,李翔检查)