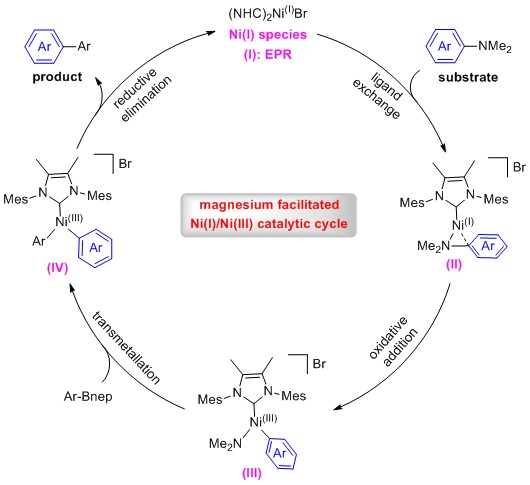
N,N-二烷基芳基胺是许多天然产物、药物和有机材料的核心骨架,因此引起了许多合成化学家的关注。在过去的几十年里,已经发展了许多高效的方法来构建芳香C-N键,如:Ullmann偶联、Buchwald-Hartwig胺化和C-H胺化等。然而产物的应用问题却一直未解决,其原因在于N,N-二烷基芳基胺具有热力学和动力学上的稳定性,并且底物和原位生成酰胺都具有较强的配位能力。
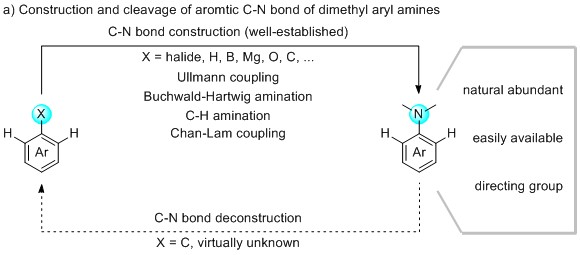
鉴于有机硼试剂具有商业可用性、稳定性和无毒性的特点,因此,Kakiuchi及其同事采用过渡金属催化的Suzuki-Miyaura偶联(SMC)策略,使用含有导向基团的N,N-二甲基芳基胺为模型底物,在过渡金属钌催化下,与芳基硼酸酯反应高效构建了碳-碳键,一定程度上推动了N,N-二甲基芳基胺的应用研究。然而,对于不含导向基团的简单N,N-二甲基芳基胺通过SMC策略构建碳-碳键并未实现,基于此,复旦大学施章杰教授通过金属镍和卡宾为催化体系,在金属镁作为还原剂的条件下,使用N,N-二甲基芳基胺和芳基硼酸酯为原料,进行交叉偶联反应直接构建了碳-碳键,该方法的优点在于原料易得和不需要导向基团协助。
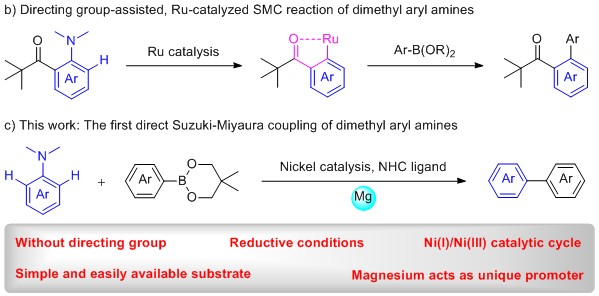
作者为了进一步了解反应机理,进行了EPR分析和DFT计算,并提出可能的反应机理:首先Ni(I)物种Ⅰ与N,N-二甲基芳基胺进行配体交换得到Ni(I)物种Ⅱ,接着进行氧化加成得到Ni(III)物种Ⅲ,随后与芳基硼酸酯进行转金属化得到Ni(III)物种Ⅳ,最后经还原消除得到目标产物,完成催化循环。(J. Am. Chem. Soc. 2018, 140, 13575.) (推荐人:李翔)