手性哌啶是一种重要的结构单元,广泛存在于生物活性分子和医药中,因此其不对称合成受到科研工作者的广泛关注,然而发展一种条件温和、更简洁有效的策略构建手性哌啶仍是迫切需要的。
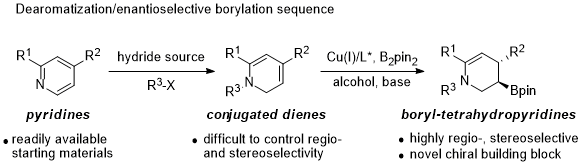
芳香杂环化合物的不对称去芳构化反应是构建手性杂环化合物的一种非常有效的策略,2015年,Ito小组报道了一价铜催化吲哚化合物硼基化去芳构化反应合成3-硼基吲哚啉化合物,得到的手性氮杂环有机硼化合物可广泛应用到合成和医药化学中。基于手性C-B键的重要意义,Ito小组最近又报道了手性硼基哌啶化合物的合成,以简单易得的吡啶作为起始原料,经Fowler小组报道的还原方法得到1,2-二氢吡啶化合物(该化合物不稳定,分离提纯后需立即投入下步反应中),随后在CuCl/(R,R)-QuinoxP催化下发生硼基化反应以高立体选择性和对映选择性实现手性硼基-四氢吡啶化合物的合成,该产物可轻松转变成抗抑郁药帕罗西汀。 (J. Am. Chem. Soc. 2016, 138, 4338-4341.)