环丙烷作为重要的结构骨架,广泛存在于具有生物活性的天然产物和药物中。因此,许多科学家致力于功能化环丙烷骨架的合成。在各种合成策略中,通过过渡金属卡宾中间体与烯烃的环丙烷化反应是一种有效直接的方法。反应中的金属卡宾物种,通常通过过渡金属催化促进的重氮羰基化合物的分解原位生成的。但很遗憾的是,高能重氮化合物具有潜在爆炸性。此外,重氮底物的制备通常需要危险的试剂和多个合成步骤。因此,开发操作安全且易于获得的重氮羰基化合物替代品作为卡宾前体显得尤为重要,特别是对于工业规模的合成。
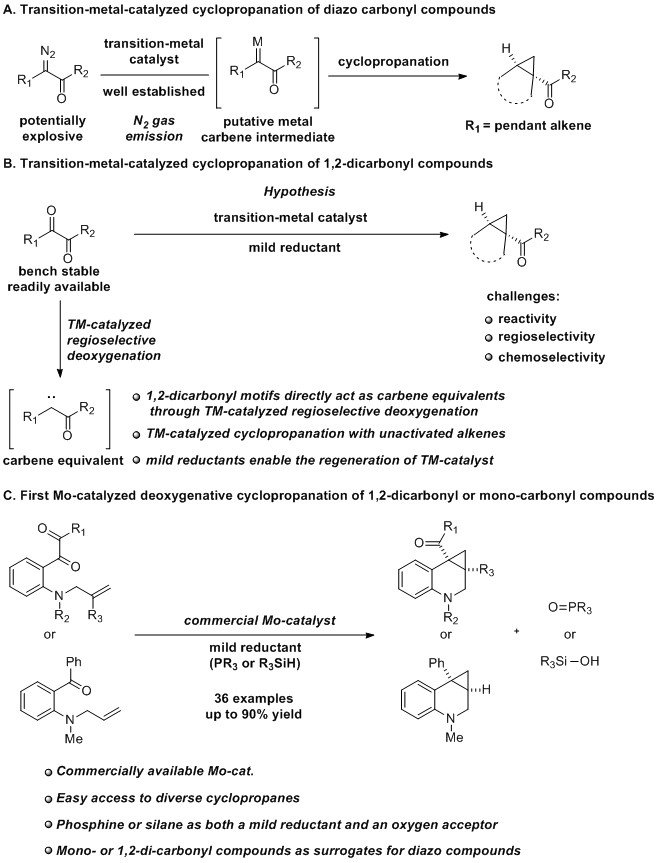
1,2-二羰基化合物很容易获得并且经常作为有机合成中的重要骨架。具体来说,这些稳定的化合物可用于制备α-重氮羰基化合物。相应地,我们设想1,2-二羰基化合物是否可以通过过渡金属催化的区域选择性脱氧反应直接作为卡宾等价物用于合成环丙烷,从而避重氮化合物的制备和使用。虽然在设计上概念很简单,但想实现过渡金属催化的区域选择性脱氧环丙烷化反应需要满足如下几点要求。首先,必须确定一种强大的过渡金属催化剂,它能够实现1,2-二羰基化合物的区域选择性脱氧,并且能抑制副反应的发生(如二聚或竞争性C-H键插入)。此外,必须找到一类不会直接还原1,2-二羰基化合物,但可以还原过渡金属氧化物的温和还原剂。通过过渡金属催化1,2-二羰基化合物的区域选择性脱氧生成卡宾等价物是具有挑战性的。在实践中,羰基化合物很少用作卡宾的直接前体,除非使用化学计量的金属试剂和还原剂或低价过渡金属配合物。据我们所知,通过过渡金属催化1,2-二羰基化合物的区域选择性脱氧生成卡宾等价物,随后与未活化的烯烃发生环丙烷化反应,还没有相关文献报道。厦门大学的卓春祥教授报道了第一个Mo催化的1,2-二羰基或单羰基化合物的脱氧环丙烷化反应。通过使用有机膦或硅烷作为还原剂,在市售的钼催化剂作用下合成一系列取代的环丙烷骨架,反应最高可以实现90%的收率和专一的区域选择性。
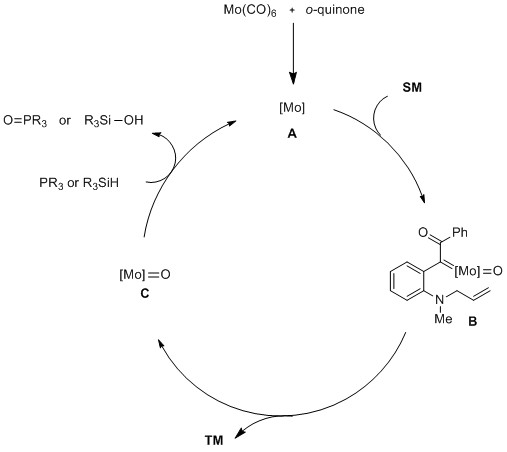
作者提出的反应机理如下:首先,底物在[Mo]配合物A作用下发生区域选择性的碳氧双键断裂生成金属钼卡宾中间体B。然后,该中间体B发成协同的分子内环丙烷化反应得到目标产物,并释放出高价的钼氧化合物C。最后,用膦或硅烷作为还原剂还原高价的钼氧化合物C再生低价[Mo]配合物A,完成催化循环。(Angew. Chem. Ind. Ed. 2021, ASAP. doi.org/10.1002/anie.202103429) (推荐人:王晓清) (检查:丁艺璇)