吲哚类生物碱具有广泛的生物活性和药理活性,近年来对于不对称合成吲哚类生物碱的研究主要集中在C3位亲核性的吲哚类化合物与亲电试剂的反应上。相对而言,将吲哚转化为亲电试剂研究较少。目前,达成吲哚电性翻转的策略主要包括在吲哚类化合物结构中引入强吸电子基和离去基团等。直接将吲哚C3位极性反转是一种新型的去芳构化方法,但少数利用例如光氧化和电氧化的吲哚氧化极性反转的案例则需要依赖于过渡金属发色团或预氧化的亲核试剂。
近日,Ishihara小组报道了一种次碘酸季铵盐催化的2,3-二取代吲哚氧化极性反转的对映选择性去芳构化方法来合成相应的螺假吲哚。该小组选用位阻较大,可以避免直接与底物发生偶联的过氧化氢异丙苯作为氧化剂。并筛选了手性季铵盐和溶剂,确定了最优条件,实现了一系列螺假吲哚的合成扩展。

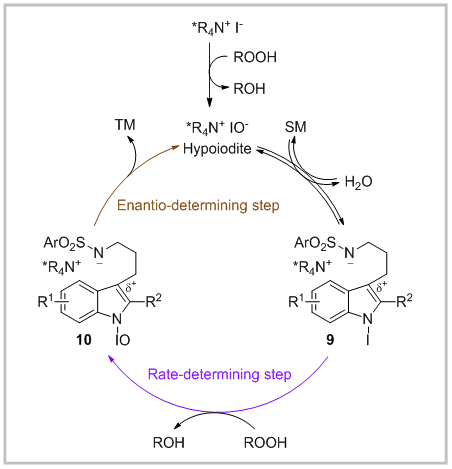
最后,作者给出了该反应的机理:首先,手性季铵盐与氧化剂原位生成次碘酸铵,随后通过次碘酸盐与吲哚N-H直接发生可逆碘化反应或通过磺胺N-H的碘化然后进行分子内碘转移产生N-I中间体化合物9。由化合物9到化合物10的氧化过程为反应的决速步骤。最后,手性磺酰胺对高亲电性中间体10进行分子内捕获,作为对映选择性决定性步骤,得到目标产物。
Reference: Tanaka, H.;Ukegawa, N.;Uyanik, M.; Ishihara, K.* Hypoiodite-Catalyzed O-xidative Umpolung of Indoles for Enantioselective Dearomatization J. Am. Chem. Soc. 2022, 144, 5756−5761 (推荐人:陈简;检查人:刘正)