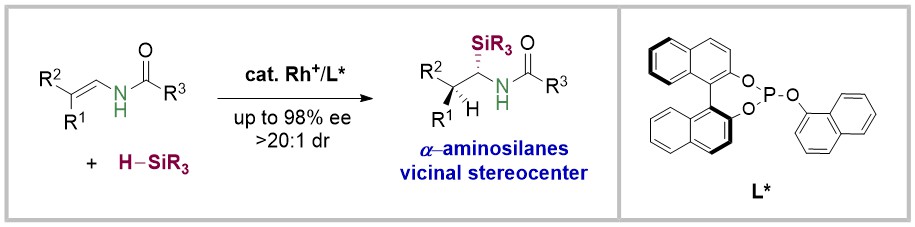
手性有机硅化合物能发生多样的官能化,因此在有机合成中具有重要价值。除此之外,含硅分子具有低毒性和良好的代谢特性,使其在药物化学领域备受关注。此外,手性α-氨基硅烷是多种有效蛋白酶抑制剂的关键结构单元。因此开发实用性的手性α-氨基硅烷合成方法是十分必要的。最近,清华大学李必杰课题组报道了铑催化β,β-二取代烯酰胺的不对称硅氢化反应,以高的区域选择性、非对映选择性和对映选择性,以及高原子经济性的方法合成了一系列手性α-胺基硅烷化合物。
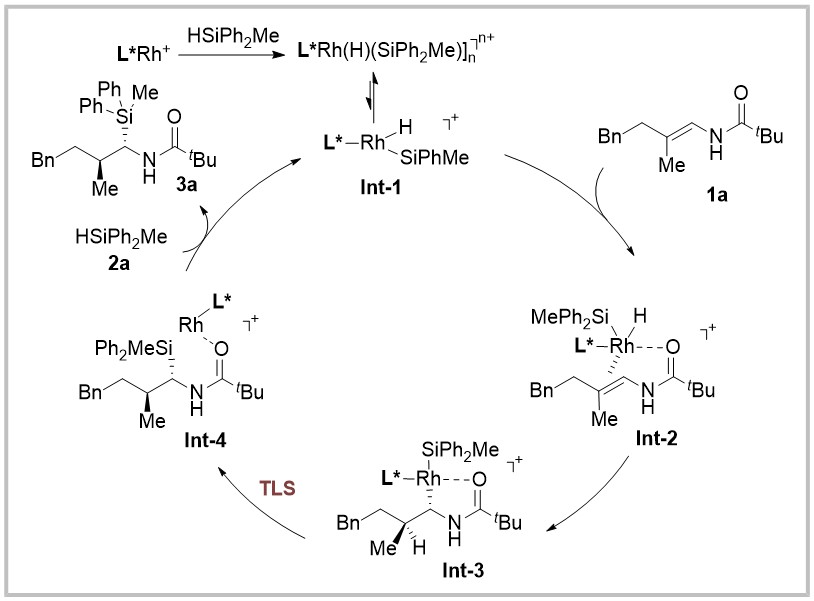
作者进行相关机理实验后,结合以往研究报道提出如下反应机理。首先,一价铑与氢硅物种进行氧化加成得到硅基铑氢中间体Int-1,该中间体可能形成二聚体或多聚体。随后,金属铑与烯酰胺1a进行螯合配位得到中间体Int-2。再经过铑氢键对烯烃的迁移插入,得到中间体Int-3,其中Int-3因酰胺配位而稳定。随后,Int-3发生还原消除形成C-Si键,生成Int-4。最后与2a配体交换释放目标产物,同时再生活性铑催化剂;其中还原消除步骤是该反应的对映选择性控制步骤。
Reference: Zhang, W.-W.; Li, B.-J. Enantioselective Hydrosilylation of β,β-Disubstituted Enamides to Construct α-Aminosilanes with Vicinal Stereocenters. Angew. Chem. Int. Ed. 2022, 62, e202214534.(推荐人:于艳江;检查人:刘正)