有机硼酸酯因其相对稳定、无毒的特性并且可通过一系列成熟的反应完成从C-B到C-X的转化而成为了合成中有用的结构单元。在结构多样的有机硼酸酯中,同位二硼酸酯和邻位二硼酸酯由于分子中的两个C-B键可以选择性地转化,最近在多步合成中受到越来越多的关注。因此,通过各种金属催化的二氢硼酸酯反应,从易于获得的不饱和烃出发获取同位二硼酸酯和邻位二硼酸酯的合成方法已被充分开发。
除了同位二硼酸酯和邻位二硼酸酯外,不相邻的二硼酸酯,例如1,3-和1,4-二硼酸酯,也是可以用作合成前体来制备各种1,3-和1,4-双官能化产物的多功能试剂。更重要的是,利用这些不相邻的二硼酸酯中两个硼基位点的区别,可以通过连续和选择性的C-B键转化实现分子官能化。由于苄基硼酸酯和烷基硼酸酯在Suzuki-Miyaura偶联和氧化反应等各种转化中表现出不同的反应性,含有苄基和烷基取代硼基位点的不相邻二硼酸酯对于正交合成尤为重要。然而,直接合成不相邻二硼酸酯的方法是有限的。因此,仍然需要寻找合适的底物和可靠的催化条件来模块化合成不相邻二硼酸酯。近日,葛少中课题组报道了第一例钴催化配体调控区域发散性亚基基环丙烷的开环双硼氢化反应合成多种1,3-和1,4-二硼酸酯化合物,并且具有非常高的化学选择性和区域选择性。
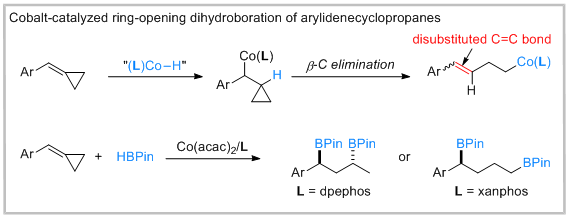
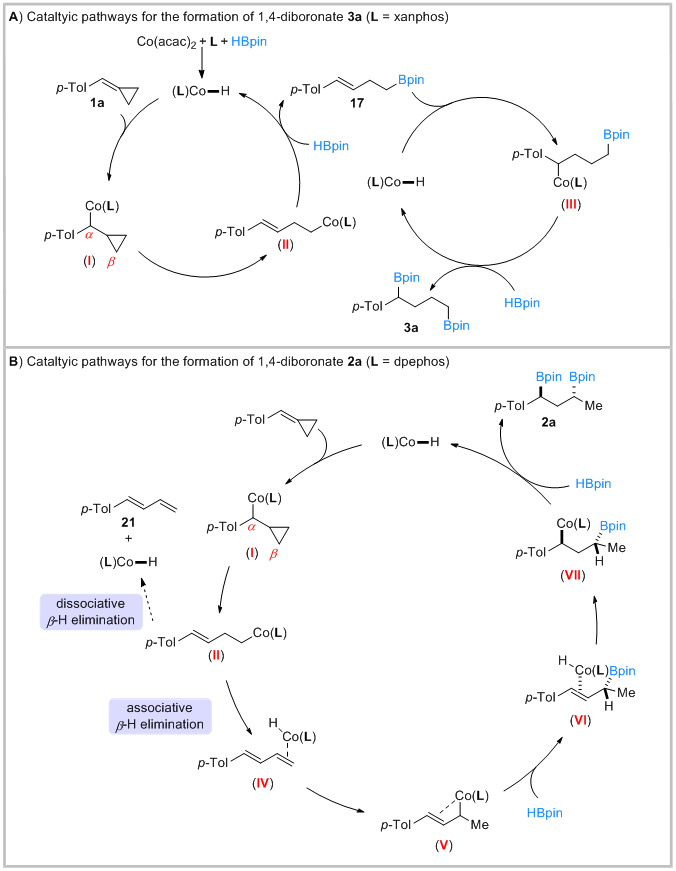
基于实验结果和文献报道,作者提出了如下可能的机理:A) 芳基环丙烷1a与HBpin在钴催化下开环二硼氢化反应的合理途径。首先,钴氢物种与底物1a发生选择性插入形成苄基钴中间体I,然后经过β-C消除以产生钴物种II,接着再与1a与HBpin反应生成硼酸酯17。17进一步与钴氢物种发生插入反应产生苄基钴中间体III。最后,该中间体与HBpin反应生成1,4-二硼酸酯产物3a并再生钴氢物种。
B)对于Co(acac)2/dpephos催化过程,柔性的配体使钴中间体II能够容易的与底物形成Co-C-C-H共面的过渡态,利于中间体II发生随后的β-H消除,形成二烯配位的钴氢物种IV。然后钴氢物种再一次插入到二烯中生成烯丙基钴物种V,接着与HBpin反应产生烯丙基硼酸酯配位的钴氢物种VI,其中钴从其双键的位阻较小一面与烯丙基硼酸酯结合。随后将配位的烯丙基硼酸酯分子插入VI的钴氢键中,生成苄基钴中间体VII,然后中间体VII与HBpin进行σ键复分解,形成1,3-二硼酸产物2a,催化活性物种钴氢得到再生。
Reference: Tan, B. B.; Hu, M.; Ge, S.*Cobalt-Catalyzed Regiodivergent Ring-Opening Dihydroboration of Arylidenecyclopropanes to Access Skipped Diboronates. Angew. Chem. Int. Ed. 2023, 62, e202307176 (推荐人:汤淏;检查人:李翔)