C-S键广泛地存在于蛋白质、天然产物、药物和有机材料中。近些年来,随着各种类型硫试剂的开发与利用,过渡金属催化的C-S键交叉偶联反应已成为构建硫醚的重要策略。但是与过渡金属催化C(sp2)-S偶联反应相比,构建具有挑战性的C(sp3)-S键仍然存在很大问题,这可能是因为反应中存在潜在的β-H消除和烷基卤代物与金属反应相对困难造成的。因此,开发一种有效且通用的方法,在温和条件下利用廉价易得的有机硫试剂来构建C(sp3)-S键在生物学上具有重要意义。
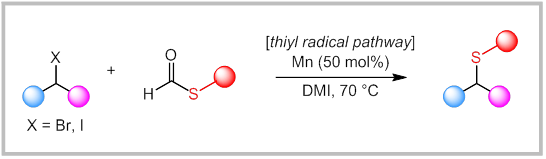
最近,南京师范大学陈良安课题组报道了一例温和条件下锰催化的烷基卤化物与硫代甲酸酯的C(sp3)-S交叉偶联反应,该反应具有反应条件温和、底物范围广等特点,且使用该策略可对复杂天然产物和药物进行后期硫醚化,进一步印证了其实用性,拓展了有机硫化学合成方法的多样性,为有机硫化合物的合成提供了新的思路。
通过一系列机理实验,作者提出了两种可能的反应机理:路径a,首先Mn0与烷基溴化物发生氧化加成生成中间体A。与此同时硫代甲酸酯在DMI和加热到70度条件下生成了甲酰基自由基和巯基自由基。中间体A和巯基自由基反应生成中间体B,之后还原消除得到目标产物3和中间体C,中间体C与甲酰基自由基相互作用生成中间体D。随后释放CO并再生Mn0,再次催化循环。路径b,Mn0也可以先与巯基自由基反应生成中间体E,再与烷基溴化物1发生氧化加成生成中间体B。
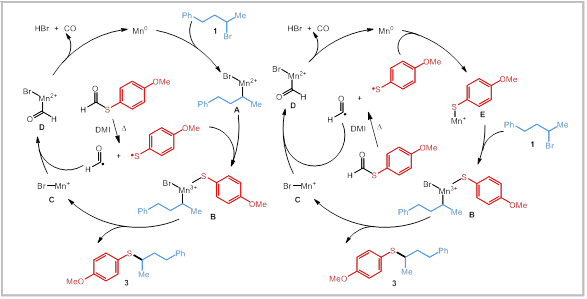
Reference: Pei, P.; Zhao, M.; Song, L.; Chen, L. Manganese-Catalyzed Redox-Neutral Thiolation of Alkyl Halides with Thioformates. Angew. Chem. Int. Ed. 2023, 62, e202305510 (推荐人:赵宝乾,检查人:牛童)