多取代吲哚常见于各种小分子药物与活性天然产物中,因此高效的吲哚官能化方法对于药物研究具有重要价值。利用现有的方法在吲哚的C2与C3位点选择性引入两个不同的碳取代基仍然是一个艰巨的挑战。目前已报道的策略主要依靠预官能化的底物通过多步反应或转化来实现。因此,开发一种直接的、模块化的和位点选择性的吲哚邻位双碳官能团化方法具有重要意义。
最近,钯/降冰片烯(Pd/NBE)协同催化已成为芳香化合物和烯烃的位点选择性官能化的有效方法。该过程通过形成芳基-降冰片基-钯环(ANP)中间体,然后与亲电试剂和亲核试剂(或烯烃)进行化学选择性偶联,实现邻位双官能化。虽然经典的Pd/NBE催化(即Catellani反应)是由Pd(0)介导的氧化加成引发的,但自Thorsten Bach和焦雷等人的开创性发现以来,Pd(II)引发的反应受到越来越多的关注并得到了广泛的应用。Pd(II)引发的反应具有如下优点:能够容忍空气和湿度,以及可以使用较少官能化的底物等。在前期研究的基础上,董广彬教授和刘鹏教授课题组发展了一种Pd(II)引发的吲哚直接邻位双碳官能团化的方法,该方法具有位点选择性高、模块化和空气耐受性好等特点。桥头取代的降冰片烯(N2)促进了这一过程,并且C1位环已基取代的降冰片烯催化效果最佳。
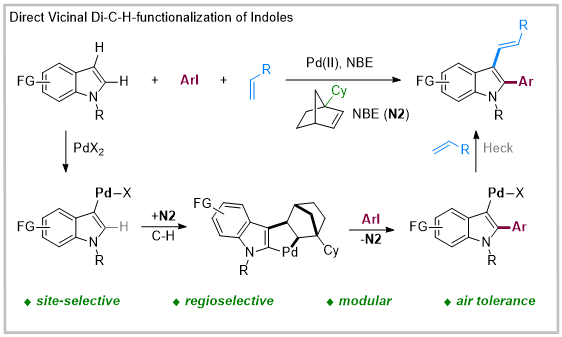
随后,作者通过实验和DFT计算对该反应的机理进行了详细研究。反应由二价钯启动,首先在吲哚底物1的C3位发生C-H键活化过程得到中间体2,之后对NBE插入并诱导吲哚C2位的第二次C-H钯化得到4。此后,钯对芳基碘化物进行氧化加成得到中间体5,随后发生还原消除得到6。6发生β-碳消除再生NBE后得到7,7与丙烯酸酯发生Heck反应得到目标产物邻位双碳官能团化吲哚8,同时生成零价钯,零价钯经氧化剂氧化再生二价钯,完成催化循环。实验和计算研究共同表明,C1取代的降冰片烯(N2)在促进4的氧化加成中起着关键作用。
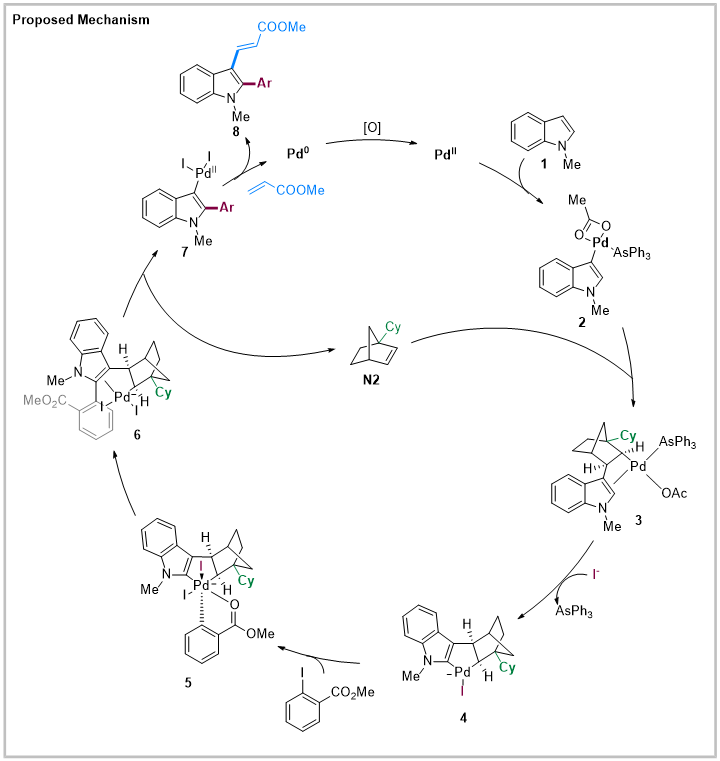
Reference: Liu, X.; Zhou, Y.; Qi, X.; Li, R.; Liu, P.; Dong, G.* Palladium/Norbornene-Catalyzed Direct Vicinal Di-Carbo-Functionalization of Indoles: Reaction Development and Mechanistic Study Angew. Chem. Int. Ed. 2023, e202310697
(推荐人:汤淏,检查人:白雨晴)