炔丙醇及其衍生物是有机合成中的重要起始原料,其在有机或金属催化下可发生多种转化,例如,与过渡金属钯或镍发生氧化加成可生成炔丙基类亲电中间体,当亲核试剂进攻炔丙基亲电中间体的不同反应位点时可实现炔丙基化、联烯基化、二烯基化和烯基化反应。
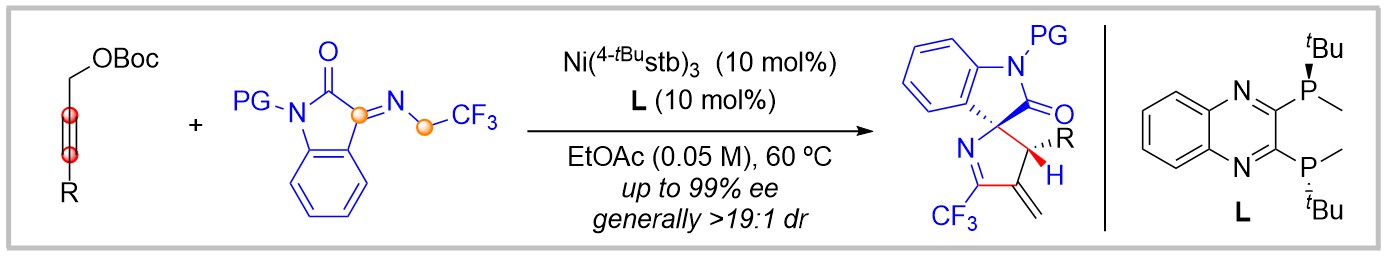
过渡金属催化炔丙醇衍生物的烯基化通过双亲核进攻的反应模式为复杂烯烃骨架的构建提供了高效的方法。然而,可能的竞争反应途径以及难以同时精准控制化学、区域和立体选择性导致该领域目前的发展较为有限。最近,四川大学华西药学院陈应春、杜玮和第三军医大学欧阳勤发展了首例廉价镍催化炔丙基碳酸酯与N-三氟乙基酮亚胺经连续氮杂插烯活化的不对称烯基化反应,以优异的化学、区域和立体选择性获得了(3+2)环合产物。该催化反应表现出广泛的底物适用性。
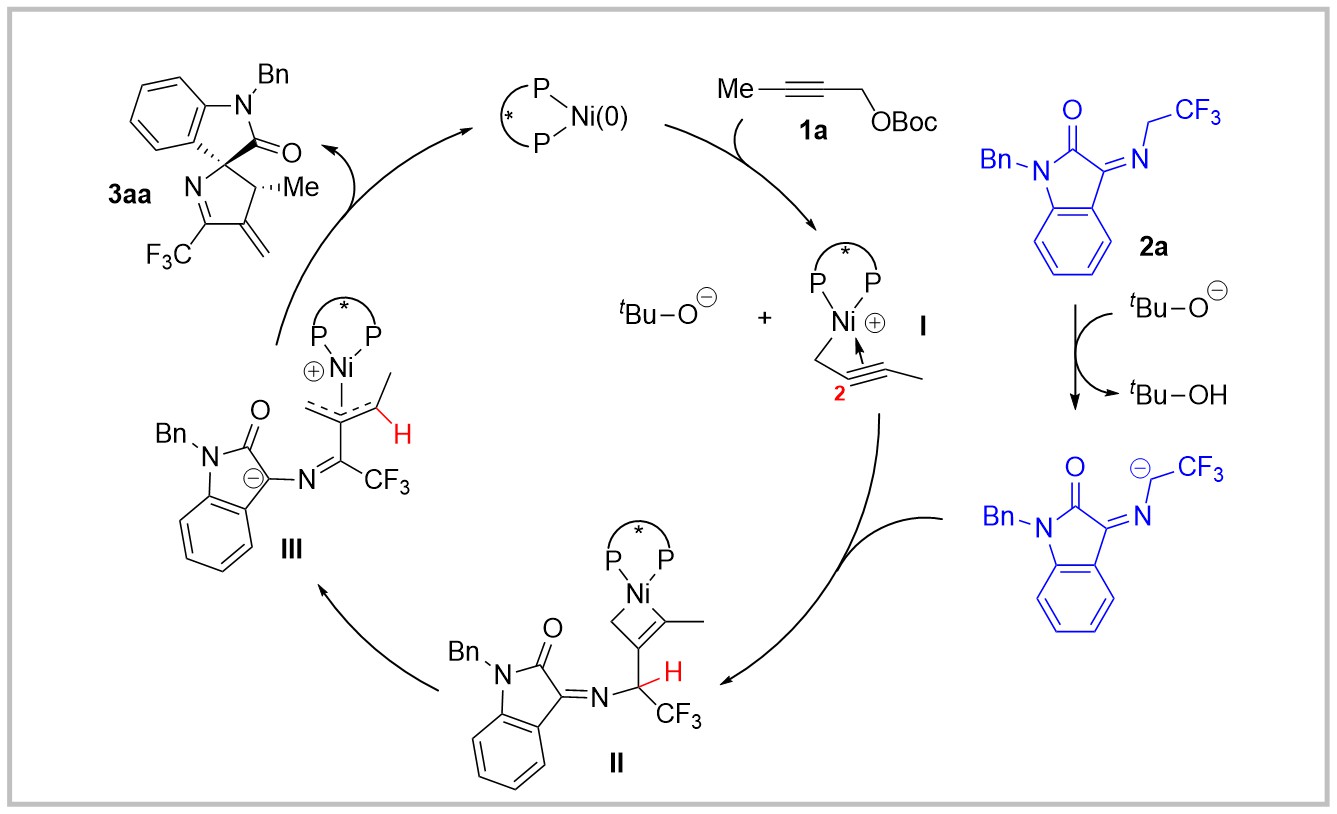
作者通过DFT计算及控制实验,提出了如下的反应机理。炔丙基碳酸酯1a首先与零价镍催化剂发生氧化加成,生成π-炔丙基镍络合物I和叔丁氧阴离子。在叔丁氧阴离子的作用下,2a发生去质子化得到2-氮杂烯丙基阴离子后,对I中的C2进行选择性亲核进攻生成镍环丁烯中间体II。由于中间体II的α-位氢具有较高酸性,易发生1,3-氢迁移得到更加稳定的顺式-π-烯丙基镍中间体III。最后经历外球型的烯丙基烷基化得到产物3aa并再生催化剂。此外,关于对映选择性和区域选择性的调控也通过DFT计算进行了详细的阐释。
Reference: Zhao, Z.; Zhu, L.; Song, Z.-L.; Qubi, K.; Ouyang, Q.; Du, W.; Chen, Y.-C. Nickel-Catalyzed Asymmetric (3 + 2) Annulations of Propargylic Carbonates and Vinylogous Donors via an Alkenylation Pathway. J. Am. Chem. Soc. 2024, 146, 30678-30685 (推荐人:史宇阳,检查人:白雨晴)