吡啶衍生物是一类重要的杂环化合物,其广泛存在于药物及生物活性分子中。在美国FDA批准的药物之中,吡啶环骨架的芳香族氮杂环化合物也是最常见的。此外,它还可以作为有机合成模块用于有机合成和配体设计。因此,含吡啶环类化合物的合成方法已引起科研工作者广泛关注。在众多已经报道的方法中,吡啶的直接碳氢官能化是一种原子经济性的方法。在这些报道中,大多数方法仅集中在消旋版本。通过碳氢键官能化来实现手性吡啶环类化合物的合成方法报道还较少。2014年, Hou课题组报道了钪催化地对映体选择性碳氢烷基化反应,该反应发生在末端烯烃取代的吡啶的2位或者6位。目前,吡啶3位和4位直接不对称碳氢官能化反应还未见报道。该方法生成的5,6,7,8-四氢喹啉(THQ)和5,6,7,8-四氢异喹啉(THIQ)化合物也是常见的生物活性分子和药物分子单元。Kuwano小组最近报道了钌催化地不对称氢化喹啉及异喹啉,可以得到5,6,7,8-四氢喹啉和5,6,7,8-四氢异喹啉化合物,对映体选择性最高为82%。最近,上海有机所的施世良课题组报道了吡啶环的对映选择性碳氢环化反应。该小组采用镍/手性卡宾催化剂催化2、3和4位含有链烯取代的吡啶,发生吡啶的碳氢烷基化反应,可得到手性的5,6,7,8-四氢喹啉和5,6,7,8-四氢异喹啉化合物,对映选择性高达99%。
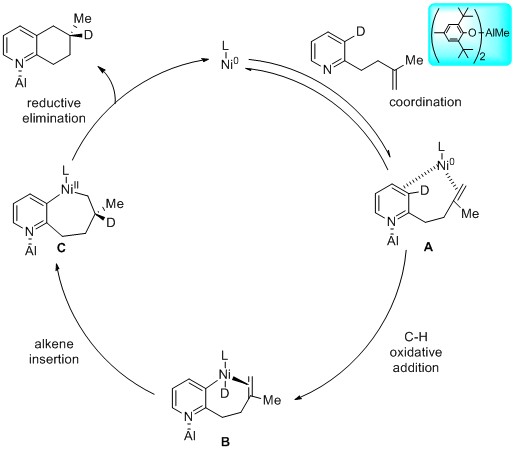
作者还对反应的机理进行了研究。(1)体积庞大的路易斯酸MAD与吡啶的氮结合,推动链状的烯烃靠近镍金属,促进η2-alkene镍络合物A的形成。(2)碳氘键断裂并与零价镍发生氧化加成形成镍氘物种B。(3)接着,发生烯烃反马氏规则的镍氢插入反应,形成七元环中间体C。(4)还原消除得到目标产物和再生镍催化剂,完成催化循环。(J. Am. Chem. Soc. 2019, 141, 5628)
赵子彪推荐