近年来,自由基交叉偶联因可简化复杂C-C键构建而备受关注。然而,传统方法依赖外源性氧化还原活化,限制了应用。
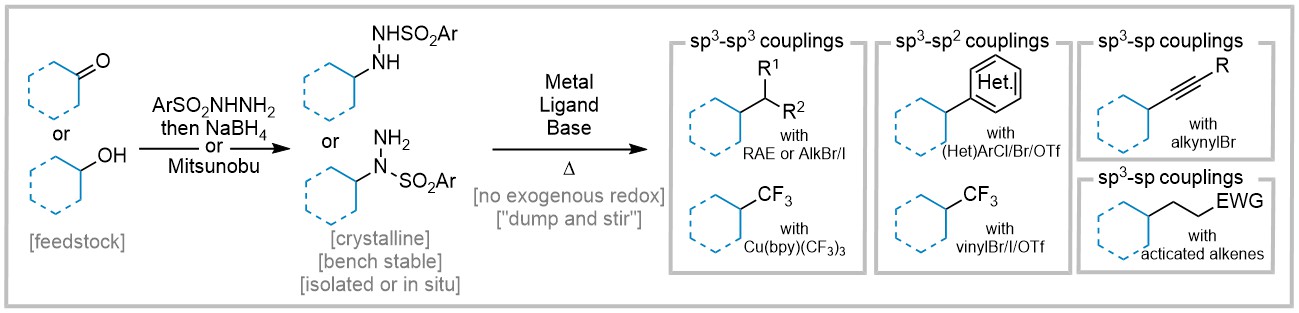
近日,美国斯克利普斯研究所Phil S. Baran团队开发了磺酰肼作为通用自由基前体,实现了氧化还原中性自由基交叉偶联反应(图1)。该策略无需化学计量添加剂或光/电化学活化,通过Ni催化体系成功构建C(sp³)–C(sp³)、C(sp³)–C(sp²)及C(sp³)–C(sp)键。研究表明,磺酰肼兼具自由基前体与电子供体功能,支持与烯烃、卤代物、三氟甲基试剂等七类底物高效偶联。一锅法操作及水相兼容性进一步提升了实用性,为药物分子(如替格瑞洛)后期修饰及复杂分子克级合成提供了新途径。
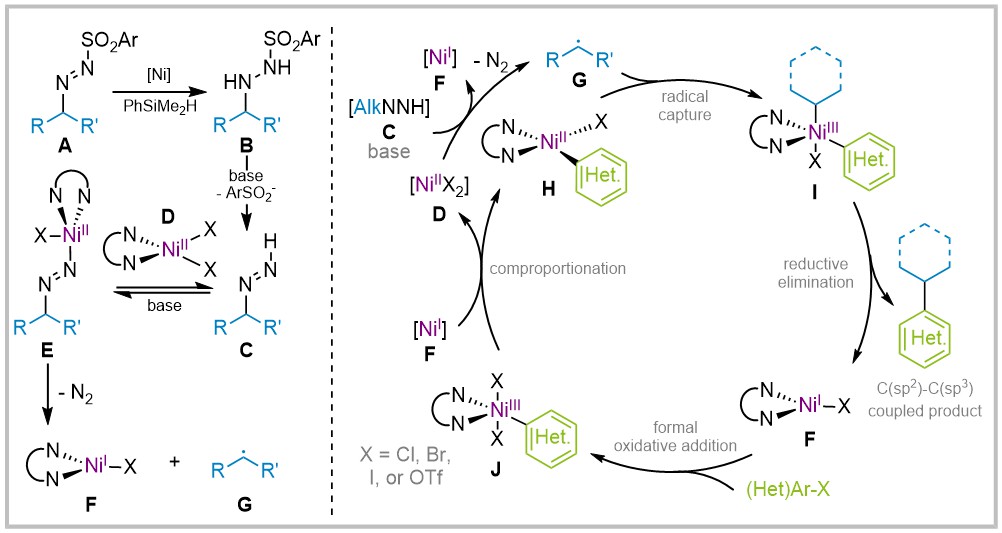
通过机理实验,作者推测了该反应可能的机理:化合物A在被镍催化转移氢化形成化合物B。化合物B进一步在碱作用下生成化合物C,其被碱攫质子后与配合物D配体交换生成配合物E。配合物E释放氮气裂解为配合物F和自由基G。配合物H捕捉自由基G得到配合物I,其随后经过还原消除得到配合物F以及目标产物。配合物F与芳基亲电试剂发生形式氧化加成得到配合物J,其最终和一价镍配合物F发生归中反应得到二价镍配合物D和H,完成催化循环。
Reference: Sun, J.; Péter, Á.; He, J.; Tsien, J.; Zhang, H.; Vokits, B. P.; Peters, D. S.; Mandler, M. D.; Palkowitz, M. D.; Kawamata, Y.; Baran, P. S. Sulfonyl Hydrazides as a General Redox-Neutral Platform for Radical Cross-Coupling Science, 2025., 10.1126/science.adu6406.