有机砜试剂,因其卓越的反应灵活性,在有机合成领域有着“化学变色龙”的美誉。通过简单地改变反应条件,可以完全改变砜试剂的反应性,使其按照合成化学家的需要分别充当亲核试剂、亲电试剂、自由基前体以及它们的组合。近年来,随着过渡金属催化的蓬勃发展,有机砜试剂在交叉偶联反应中也得到了广泛的应用。相比于传统的卤素,三氟甲磺酸酯等亲电试剂,有机砜试剂中看似不“活泼”的C-SO2键能在特定条件下被有效地转化,从而为正交偶联反应构建复杂的功能分子提供了一条有效的途径。然而,C-SO2键固有的惰性仍是这一领域固有的的挑战。目前主流的C-SO2键活化策略是通过对有机砜试剂(R-SO2R)上离去的磺酰基(SO2R)进行调控:1)通过在砜试剂上引入强拉电子基团,利用诱导效应活化C-SO2键;2)通过设计合成具有单电子氧化还原活性的有机砜试剂。这些策略不仅步骤繁琐,而且还会在反应过程中生成低活性的亚磺酸根负离子(RSO2-),致使它们无法被重新利用。也正是由于这个原因,这些反应也通常被称作是脱砜转化反应(Desulfonylative Transformations)。在很多情况下,这些离去的亚磺酸根负离子还会在反应过程中分解,亦或者是在发生偶联副反应,带来反应化学选择性上的难题。
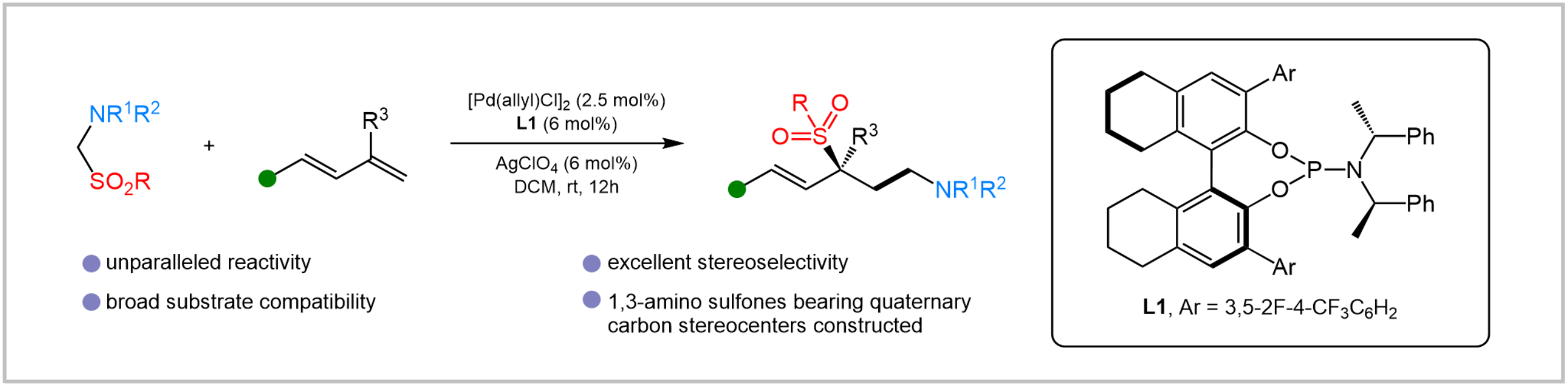
为解决这一难题,中国科学技术大学黄汉民教授团队设想:在C-SO2键相邻的碳上引入一个杂原子,利用杂原子上的孤对电子轨道与C-SO2键的成键轨道的排斥作用来活化C-SO2键,不仅无需对砜试剂(R-SO2R)的离去基团(SO2R)进行复杂的修饰,还能在温和的反应条件下实现对C-SO2键的高化学选择性切断。基于此,该课题组开发了一种新颖的胺甲基砜试剂,并基于此实现了共轭二烯的不对称胺甲基化-磺酰化反应。
机理研究方面,作者发现无论是使用N,O-缩醛和亚磺酸为原料,亦或是使用亚磺酸钠、酸以及N,O-缩醛,均可以顺利得到目标产物,展示了这一合成策略的灵活性。反应历程监测表明在上述过程中,胺甲基砜试剂作为反应的中间体会立刻生成并随着反应的进行逐渐消耗。控制实验和31P NMR研究指出:反应是通过烯丙基钯中间体与胺甲基砜试剂的协同作用来生成目标产物,同时再生三元环钯中间体的。
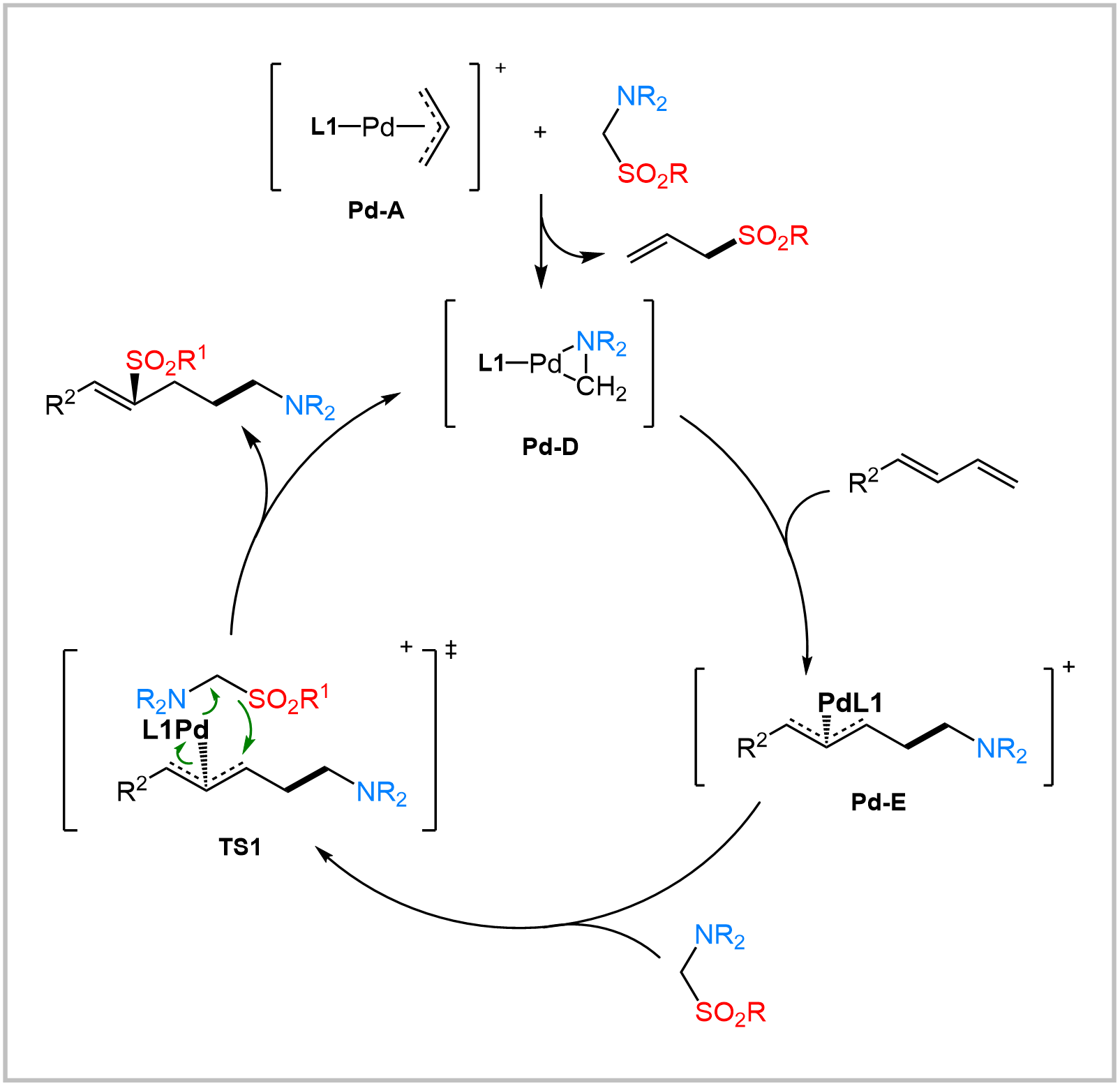
总之,中科大黄汉民教授课题组设计了一种邻位氮原子促进的C-SO2键活化策略,开发了一种新型的胺甲基砜试剂,并基于此实现了共轭二烯的不对称胺甲基化-磺酰化反应。广泛底物兼容性、高效的反应活性以及优秀的立体选择性展示了这种胺甲基砜试剂在合成化学中的巨大潜力。关于这种胺甲基砜试剂独特性质及其应用的深入研究仍在持续进行中。
Reference: Cai, S.; Zhao, Z.; Yang, G.; Huang, H.* A Bifunctional Sulfone Reagent for Asymmetric Aminomethylative Sulfonylation of Dienes. Journal of the American Chemical Society 2025, 147, 32, 28624–28631.(推荐人:李昕阳,检查人:薛凯)